|
Nombre Atomique |
7 |
Conductibilité thermique |
0,0258 W m-1 K-1 |
|
Groupe |
15 |
Rayon atomique |
54,9 pm |
|
Période |
2 |
Configuration électronique |
[He] 2s2 2p3 |
|
Année de découverte |
1772 |
Électronégativité |
3,04 |
|
Masse Atomique |
14,0067 |
Résistivité électrique (20 °C) |
- |
|
Nombre d’oxydation |
-3 -2 -1 +1 +2 +3 +4 +5 |
État physique (20 °C) |
Gaz incolore |
|
Densité (g dm-3) |
1026 (21 K)
|
Volume molaire (cm3 mol-1) |
13,65 (21 K) |
|
À l’état Naturel |
N2 |
Molécule courante |
NaNO3 |
Propriétés thermiques |
|||
|
Point de fusion |
-210,00 °C |
Enthalpie de fusion |
0,72 kJ mol-1 |
|
Point d'ébullition |
-195,8 °C |
Enthalpie d'évaporation |
5,577 kJ mol-1 |
|
Température critique |
-146,96 °C |
Chaleur d'atomisation |
470,842 kJ mol-1 |
Énergie d' ionisation et abondance |
|||
|
Énergie de 1er ionisation |
1402,34 kJ mol-1 |
Abondance (air) |
780900 ppm |
|
Énergie de 2ème ionisation |
2856,11 kJ mol-1 |
Abondance (croûte terrestre) |
20 ppm |
|
Énergie de 3ème ionisation |
4578,19 kJ mol-1 |
Abondance (océans) |
0,8 ppm |
|
Potentiel(s) d'ionisation |
14,53; 29,60; 47,45 eV |
|
|
|
Propriétés nucléaires |
|||
|
Isotope |
Masse atomique |
Abondance (%) |
Masse volumique à 20 °C |
|
14N 15N |
14,003074005 15,000108898 |
99,634 0,366 |
1,17 g/dm3 à 101,3 kPa |
|
|
|
|
|
|
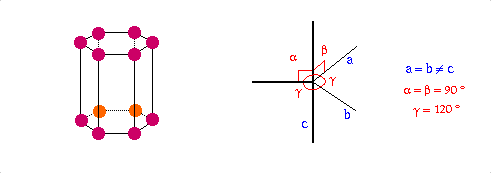
Structure cristalline |
Hexagonale
|
|
a=404.2, c=660.1
P63/mmc |