|
Nombre Atomique |
30 |
Conductibilité thermique |
116 W m-1 K-1 |
|
Groupe |
12 |
Rayon atomique |
133,5 pm |
|
Période |
4 |
Configuration électronique |
[Ar] 3d10 4s2 |
|
Année de découverte |
1746 |
Électronégativité |
1,65 |
|
Masse Atomique |
65,39 |
Résistivité électrique (20 °C) |
5,964 μΩcm |
|
Nombre d’oxydation |
+2 |
État physique (20 °C) |
Solide gris pâle bleuté |
|
Densité (g dm-3) |
7133 (293 K)
|
Volume molaire (cm3 mol-1) |
9,17 (293 K)
|
|
À l’état Naturel |
|
Molécule courante |
ZnO |
Propriétés thermiques |
|||
|
Point de fusion |
419,53 °C |
Enthalpie de fusion |
6,67 kJ mol-1 |
|
Point d'ébullition |
907 °C |
Enthalpie d'évaporation |
114,2 kJ mol-1 |
|
Température critique |
3107 °C |
Chaleur d'atomisation |
130,181 kJ mol-1 |
Énergie d' ionisation et abondance |
|||
|
Énergie de 1er ionisation |
906,41 kJ mol-1 |
Abondance (air) |
- |
|
Énergie de 2ème ionisation |
1733,31 kJ mol-1 |
Abondance (croûte terrestre) |
80 ppm |
|
Énergie de 3ème ionisation |
3832,71 kJ mol-1 |
Abondance (océans) |
0,01 ppm |
|
Potentiel(s) d'ionisation |
9,39; 17,96; 39,72 eV |
|
|
|
Propriétés nucléaires |
|||
|
Isotope |
Masse atomique |
Abondance (%) |
Masse volumique à 20 °C |
|
64Zn 66Zn 67Zn 68Zn 70Zn |
63,929147 65,926037 66,927131 67,924848 69,925325 |
48,6 27,9 4,1 18,8 0,6 |
7,14 g/cm3 |
|
|
|
|
|
|
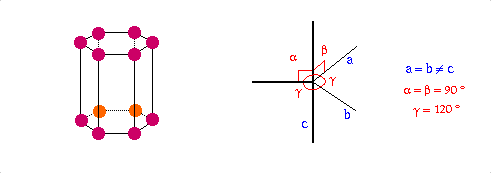
Structure cristalline |
Hexagonale |
|
a=266.47, c=494.69
P63/mmc |